II.1.8. Izvodljivost dobijanja grupe platinskih metala iz Anodnog mulja
Grupi
platinskih metala pripada šest prelaznih elemenata, koji se u periodnom sistemu
elemenata nalaze u petoj i šestoj periodi neposredno ispred srebra
i zlata.
To su rutenijum (Ru), rodijum
(Rh), paladijum
(Pd), osmijum (Os), iridijum (Ir) i platina (Pt).
Platinski
metali imaju slične hemijske osobine, a zajednička im je velika otpornost na
delovanje većine hemijskih sredstava. Otporni su na habanje i gubitak sjaja što
ih čini (pogotovo platinu) pogodnim za izradu nakita, te imaju odlične
visoko-temperaturne karakteristike i stabilna električna svojstva. U rastvorima
stvaraju veliki broj kompleksnih jona. Takođe, stvaraju koordinacijska
jedinjenja sa ugljen-monoksidom i drugim pi-vezujućim
ligandima. Postoji i veliki broj kompleksa u kojima je vodonikov atom direktno povezan sa metalom.
Platinski metali i njihova jedinjenja imaju veliku katalitičku aktivnost.
Platina, legure platine i iridijum koriste se kao materijali za izradu reaktora za rast monokristala, naročito oksida.
Hemijska industrija koristi znatne količine katalizatora od platine ili legure platine i rodijuma za kataliziranje delimične oksidacije amonijaka,
čime se dobija azot oksid - sirovina za veštačka đubriva, eksplozive i azotnu kiselinu.
U poslednje vreme platinski metali su postali važni kao katalizatori u
sintetičkoj organskoj hemiji.
Proizvodnja
čistih metala platinske grupe metala obično počinje od ostatka anodnog mulja iz
koga su prethodno izdvojeni bakar, selen, telur, germanijum, srebro i zlato. Za
selektivno izdvajanje metala platinske grupe koriste se razlike u hemijskoj
reaktivnosti i rastvorljivosti jedinjenja tih metala.
Prvi
korak u dobijanju grupe platinskih metala, nakon
izdvajanja bakra, selena, telura, germanijuma, srebra i zlata iz ostataka
anodnog mulja – ostatak Dore metala jeste rastvaranje u vrućoj carskoj
vodi* uz dodatak hlora i formiranje njihovih Cl - kompleksa. Tom prilikom
rastvoriće se platina, paladijum i zaostale količine zlata, dok će osmijum, rutenijum, rodijum i iridijum ostati nerastvoreni u
čvrstom ostatku. Iz rastvora hlorida dobijaju se zlato, platina i
paladijum, dok se preostali čvrsti ostatak topi sa natrijum
bisulfatom. Tom prilikom rodijum prelazi u rastvor dok nerastvorljivi ostatak
sadrži rutenijum (Ru), osmijum (Os) i iridijum (Ir). Taj čvrsti ostatak se
tretira sa natrijum oksidom, u kome je iridijum nerastvorljiv, dok rutenijum i
osmijum formiraju rastvorne soli.
_________________________________________________________________________________
* Carska voda je smeša jedne zapremine koncentrovane azotne kiseline i tri zapremine koncentrovane hlorovodonične kiseline.
To je lako isparljiva tečnost žućkaste boje. Izuzetno je kaustična.
Ime je dobila po tome što može da reaguje sa plemenitim (carskim) metalima,
prvenstveno sa zlatom i platinom, koji ne reaguju sa drugim supstancama. Interesantno je da nijedna od
komponenata individualno ne reaguje sa plemenitim metalom. Međutim, u rastvoru,
azotna kiselina, koja je jako oksidaciono sredstv,
oksidiše u maloj meri površinski sloj npr. zlata do Au3+ katjona,
koji zatim reaguje sa hloridnim Cl1- anjonom (iz disosovane hlorovodonične
kiseline) gradeći AuCl41- anjon. Bitno je da je carska
voda bude sveže pripremljena jer zbog reakcija između koncentrovanih kiselina
gubi na jačini.
Ako
u polaznom materjalu ima prisutnog srebra, ono se odvaja formiranjem nerastvornog
srebro hlorida.
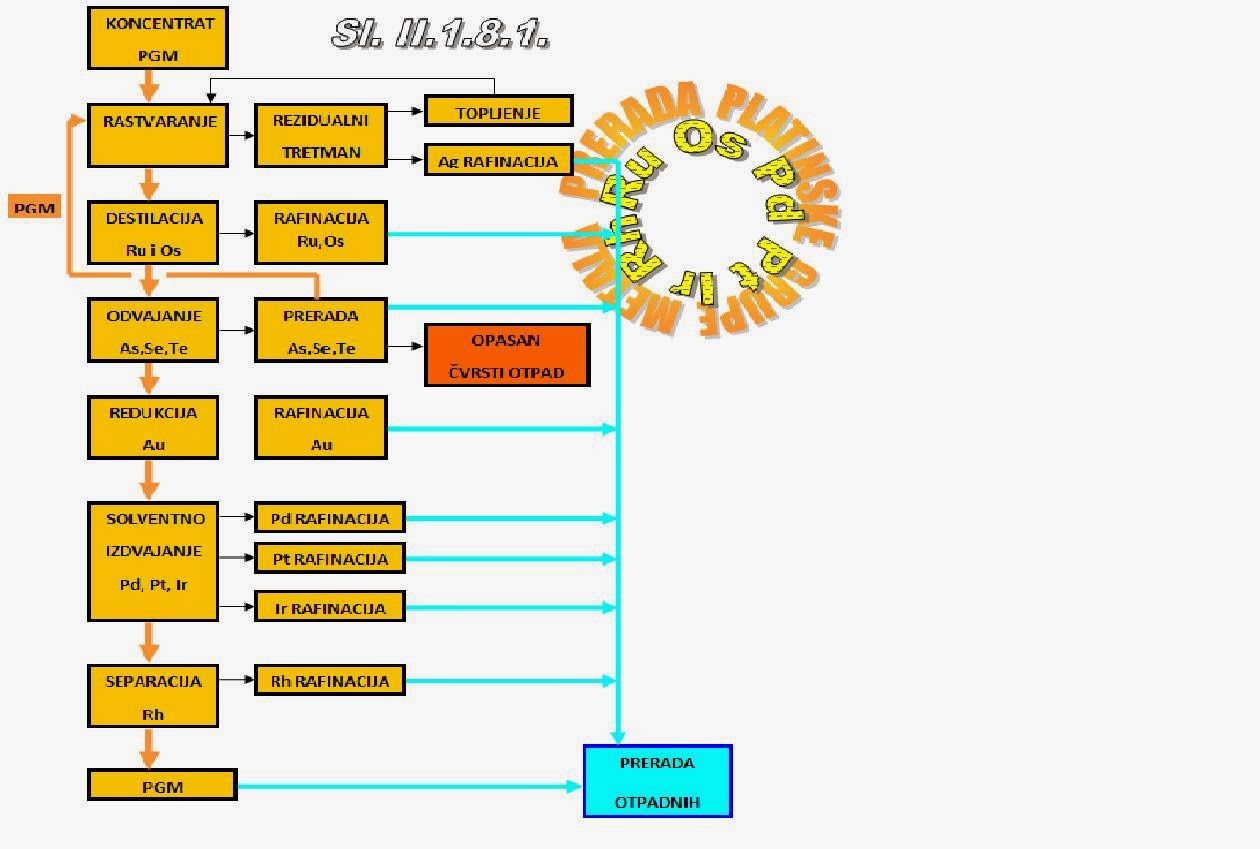
Na
sl. II.1.8.1. prikazana je Tehnološka šema izvodljivosti dobijanja grupe
platinskih metala iz anodnog mulja.









Нема коментара:
Постави коментар